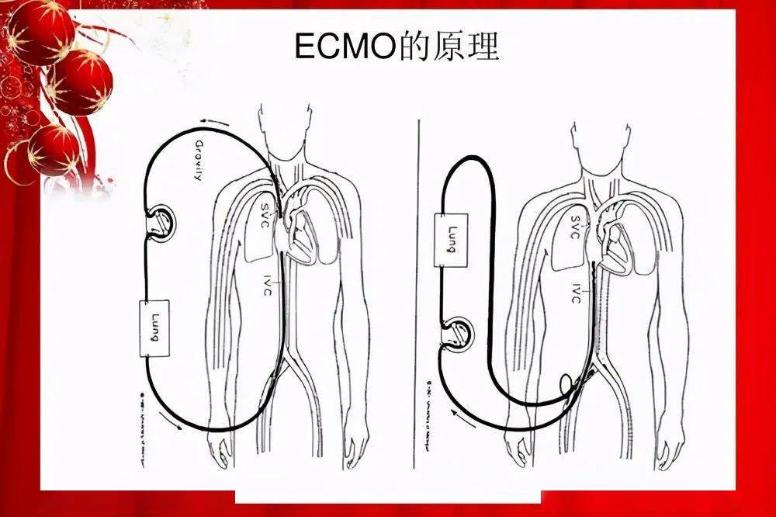
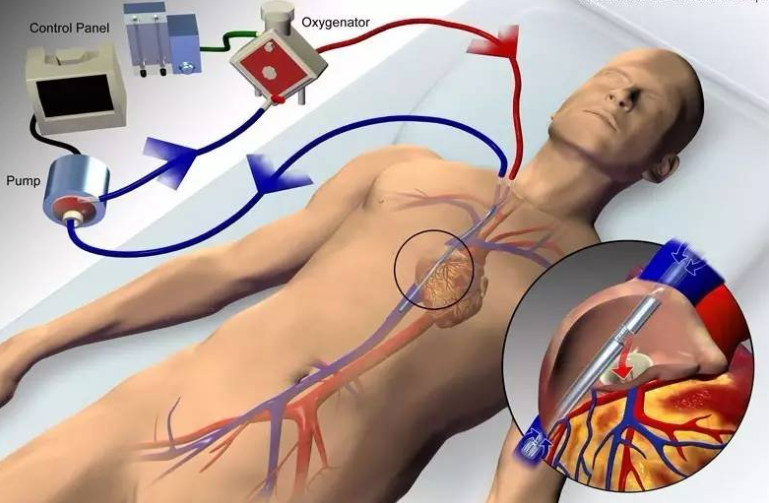
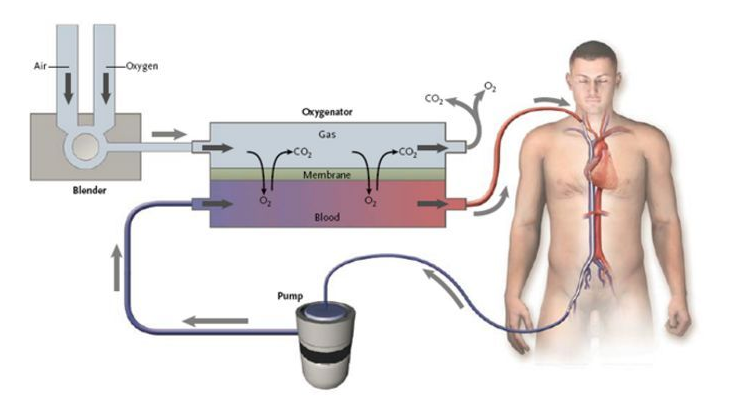
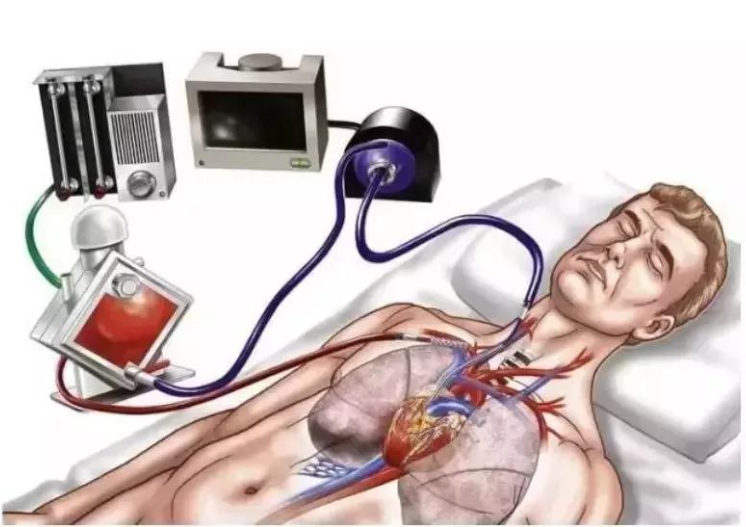
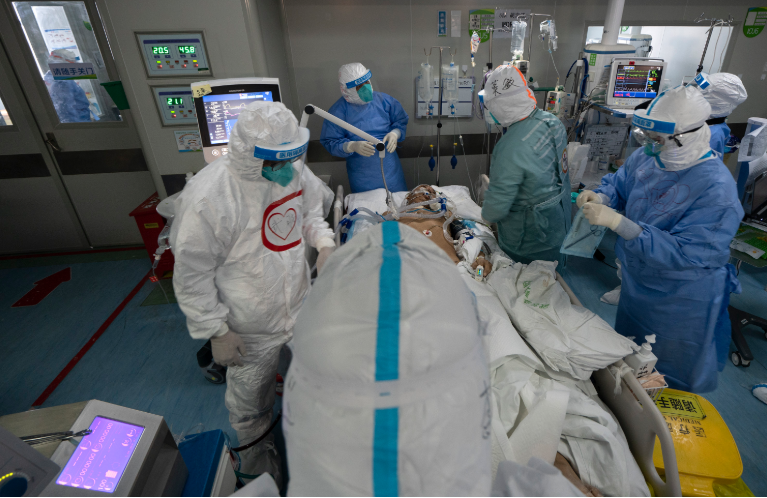
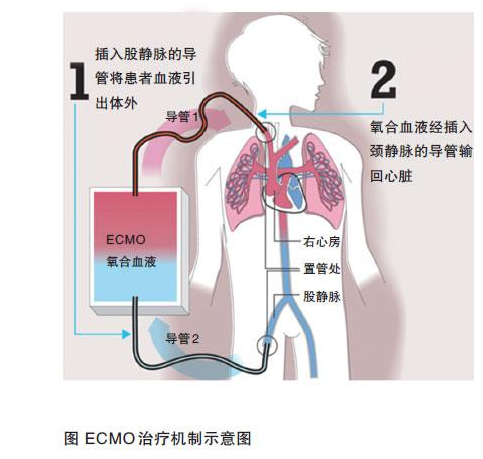
体外膜肺氧合(Extracorporeal Membrane Oxygenation,ECMO)主要用于对重症心肺功能衰竭患者提供持续的体外呼吸与循环,以维持患者生命。
精选百科
本文由作者推荐
体外膜肺氧合 相关的文章
《我和26岁美女上司》又名:《情迷美女上司》是一部都市言情小说,由欲大叔所创作,连载于看书网。故事讲述的是女朋友劈腿后,倒霉男人王文阴差阳错地招惹了火辣感性的妖媚女上司,并于酒后闯进了她的生活。
委内瑞拉国家男子篮球队,是一支南美篮球劲旅。他们曾在2005年的美洲锦标赛上以93比83战胜了美国队获得美洲杯的季军。委内瑞拉国家男子篮球队,曾参加1990年,2002年及2006年男篮世锦赛,最好成绩11名,1992年参加奥运会,获得第11名。七次参加南美男篮巡迴赛,获过一次冠军,两次亚军,三次第3名,一次第4名,
第8届亚洲冬季运动会于2017年02月19日至2017年02月26日在日本北海道的札幌和带广举行,札幌作为主办城市,带广协办,这也是札幌市第三次举办亚洲冬季运动会,日本作为东道主第四次主办亚冬会。本届札幌亚冬会设11项比赛项目。
亨克尔He-111(Heinkel He 111)是1936年开始生产的中型轰炸机,最初是为参与1932年汉莎航空快速客机的竞标而开始研发的。由于当时德国仍被《凡尔赛条约》束缚,严禁拥有各类进攻型武器,因此为了掩人耳目,德国军方授意亨克尔公司将该机型表面上设计为民用飞机,实际只需稍加改造即可成为军用轰炸机。He-111在二战后期成为落后的设计,但一直继续生产至1944年,当大部分He-111停产时,该机种开始转作用运输及补给的角色
崩密列(Beng Mealea),是一座小吴哥窟式的寺庙,名字的意思是“荷花池”。这座寺庙距离吴哥古迹群以东40公里,崩密列是一座印度教寺庙,但是它有一些雕塑都反映的是佛教的主题。建造这座寺庙最初所使用的材料是沙岩,所以很多建筑都已经损毁,而且很难再被复原。
比亚迪股份有限公司(股票代码:1211.HK),创立于1995年,2002年7月31日在香港主板发行上市,公司总部位于中国广东深圳,是一家拥有IT,汽车及新能源三大产业群的新技术民营企业。比亚迪在广东、北京、陕西、上海、天津等地共建有九大生产基地,总面积将近700万平方米,并在美国、欧洲、日本、韩国、印度等国和中国台湾、香港地区设有分公司或办事处,现员工总数将近20万人。
简介 追诉时效是指按照刑法的规定追究犯罪或者侵权行为的有效期限。犯罪行为已经超过法律规定的追诉时效期限的,不再追究其法律责任;如果已经被追究了法律责任,该案件应当予以撤销。 刑事案件追诉时效的期限是根据各种犯罪法定刑的轻重,分别规定长短不一的追诉时效期限: 1、法定最高刑为不满5年有期徒刑的,追诉时效的期限为5年; 2、法定最高刑为5年以上不满10年有期徒刑的,追诉时效期限为10年; 3、法定最高刑为10年以上有期徒刑的,追诉时效的期限为15年; 4、法定最高刑为无期徒刑、死刑的,追诉时效的期限为20年。如果20年以后认为必须追诉的,报请最高人民检察院核准后,仍然可以追诉。 特殊情况。

夜旅
还来不及增加介绍呢!
作者