概述

干细胞移植
在一定条件下,它可以分化成多种功能细胞。目前的研究结果已经证实,干细胞在适当的条件下可以分化成肌肉、骨骼、脂肪等多种体细胞、组织和器官,是再生医学的种子细胞,因此被医学界称为“万能细胞”。干细胞技术,又称再生医学技术,是近年发展起来的一种现代生物技术,是继克隆技术、基因工程之后的第三大生物科学成就。干细胞技术是指通过对干细胞进行分离、体外培养、定向诱导、甚至基因修饰等过程,在体外繁育出全新的、正常的甚至更年轻的细胞、组织或器官,并最终通过细胞组织或器官的移植实现对临床疾病的治疗。胚胎干细胞治疗旨在通过从胚胎中提取干细胞,利用胚胎干细胞能分化成所有不同种类体细胞的能力,来医治人体各类疾病。仅从技术角度说,用胚胎干细胞培养人体组织和器官以治疗疾病最为理想。
治疗机理
自体干细胞移植技术对治疗中枢神经损伤和脑损伤疾病有较好效果,其机理主要包括四个环节。
第一步移植到体内的部分干细胞,可定向分化为巨噬细胞,起到清道夫的作用,“吃掉”局部坏死的组织细胞;
第二步是在受创组织所处的环境改善后,局部血流量增加,并且局部血管系统可得以修复,可促使患者改善症状;
第三步就是把移植的干细胞定向分化为神经胶质细胞(神经细胞的“幼稚”状态);
第四步才是神经细胞的再生,包括受损神经的存活和再生以及移植的干细胞定向分化为神经细胞,新的神经环路就此重生。
据研究人员介绍,目前干细胞移植技术主要有两种方式:一是将部分干细胞直接移植到体内,由体内的信号来引导这部分干细胞分化为成熟的合适的细胞;二是他们在进行上面的移植手术的同时,也可以在病人的病灶部位安装一个干细胞移植泵,将部分干细胞在体外进行培养扩增,使之在体外向所需的方向分化,而后分批用移植泵移植到病人体内。这两种技术结合起来使用对病人的疗效最佳。
治疗流程

自体干细胞移植
自体干细胞移植
自体干细胞移植主要分为两大步,即自体干细胞的采集和干细胞的移植。
在临床上根据自体干细胞采集的方法不同分为骨髓干细胞移植和外周血干细胞移植。前者先在无菌条件下采集患者自体骨髓350~500ml,通过分离、纯化等过程,制成含有足够数量干细胞的细胞悬液;后者是给患者注射4-5天粒系集落刺激因子,以动员骨髓干细胞进入外周血,使其在外周血中达到一定数量,再用血细胞分离机分离出需要的干细胞进行移植。
我们以糖尿病和糖尿病足为例来说明干细胞的移植的过程:
利用自体干细胞移植治疗糖尿病时,我们将用以上方法制备好的干细胞悬液通过动脉导管迁移到胰腺组织中,在胰腺组织微环境的诱导下分化增殖为胰岛样细胞并分泌胰岛素。
在治疗糖尿病足时,自体干细胞移植的方法有两种:下肢肌肉局部注射和下肢动脉导管注射。两种不同的移植方法在临床上均取得了满意疗效。
首先,确认病人的外周血中没有引起疾病复发的细胞如白血病细胞、骨髓瘤细胞、淋巴瘤细胞等;
其次,对病人进行造血干细胞的动员,可以应用化疗加或不加G-CSF,动员造血干细胞到外周血来;
第三,对病人进行外周血干细胞的单采,并对之进行保存;
第四,对病人进行预处理;
第五,为病人回输外周血造血干细胞;
第六,进行支持治疗和促进造血重建的治疗
治疗优势

自体干细胞移植
自体干细胞移植
自体干细胞移植是在患者疾病缓解期或恶性肿瘤未侵犯骨髓时,将其造血干细胞分离出,经过处理清除可能残留的白血病细胞,冰冻保存,然后在放化疗预处理后输回患者体内,经过20~40天的时间,病人白细胞、红细胞和血小板及免疫功能可以完全恢复正常。这是一种相对安全、经济并适合我国国情的有效疗法,已在国内外广泛应用。据国内权威医疗机构统计,自体干细胞移植与异体干细胞移植的生存率相比相差无几。
在异体干细胞移植中,最重要的是要选择与患者相同的HLA(人类白细胞抗原)健康人造血干细胞,经放化疗预处理后移植到患者体内。人类白细胞抗原存在于人体的各种有核细胞表面,它是人体生物学的“身份证”,由父母遗传,能识别“自己”和“非己”,因而人类白细胞抗原在异体造血干细胞移植的成败中起着重要作用。但是,要在茫茫人海中寻找到和自己HLA完全匹配的人的造血干细胞是非常困难的,无异于大海捞针。相对来说,自体造血干细胞移植就不用费这样的周折,因此具有取材方便、费用少、安全性高、术后不需服用抗排异药物等特点,但自体干细胞移植也有它的治疗范围,主要适用急性白血病、恶性淋巴瘤、骨髓瘤、系统性红斑狼疮以及晚期乳腺癌患者,异体干细胞移植则主要适用于慢性粒细胞性白血病及有不良预后的急性白血病。用自身的骨髓干细胞,不需供髓者,此法简便,易于推广,可用于独生子女,并且无GVHD的发生。用于白血病,淋巴瘤和多种实体瘤的治疗。如果情况允许您可以选择自体干细胞移植。
应用现状

自体干细胞移植
自体干细胞移植
无论是何种干细胞移植都只能是经积极治疗完全缓解后(临床上无白血病所致的症状和体征、血象正常、骨髓中白血病细胞≤5%)才能进行。年龄要求是:自体<60岁,异体<45岁,无其他严重的疾病等条件都许可的情况下才可进行。对急性淋巴细胞性白血病或急性髓系白血病,如果在综合(化疗+中医药)治疗结束后的头三年没有病兆,以后复发的可能性甚小,根据临床诊断,70%~80%的儿童急淋患者并不需要进行骨髓移植。
自体干细胞移植的增加速度远远大于异基因干细胞移植到增加速度。2002年,北美4244例干细胞移植中,只有371例为异基因造血干细胞移植。1990年到2000年,欧洲造血干细胞移植病例数为132963例,其中异基因干细胞移植为44165例,占总数的33%;自体干细胞移植为88798例,占总数的67%。目前中国在造血干细胞移植领域仍然以异基因移植为主,很少应用自体干细胞移植技术。异基因干细胞移植是移植他人的干细胞,主要缺点是配型困难和移植物抗宿主反应。自体干细胞移植的大幅度增加,首先得益于特殊检验在适应症选择方面的技术突破和干细胞处理技术的进步。自体干细胞移植在许多疾病的治疗方面好于或相当于异基因干细胞移植,不需要干细胞配型,没有抗宿主反应相关的移植相关死亡等。现代干细胞或肿瘤细胞清除提供了可靠方法,这也是自体干细胞移植在国外成为主流治疗手段的原因之一。目前我国已经能够做到,以自体干细胞移植技术和实验室自体干细胞特殊处理为核心技术,治疗白血病和其他肿瘤以及糖尿病等其他免疫系统疾病。
美容应用

自体干细胞移植美发
自体干细胞移植美发
如今人们对美容的要求早已不仅仅限于割双眼皮、隆鼻等,而各种新的美容技术也层出不穷,从注射肉毒素除皱到吸脂减肥,都已经不是什么新鲜事。而且,更有人把干细胞移植技术运用到了美容领域中,达到除皱的目的。不过专家提醒爱美的人们,尝试美容新技术要慎重,因为目前很多美容技术还不成熟。
专家指出,这一技术目前存在很多问题,一是目前对于通过干细胞注射来美容除皱,还没有足够实验室依据以确定体外培养的确实是自体干细胞,国家也尚未许可其进入临床试用阶段;二是还没有确凿的实验室证据确认注射回人体的确实就是从人体中取出的干细胞;三是这一技术中干细胞在体外要经过培育,这个过程中为达到细胞增殖目的,可能会加入一些动物血清和刺激细胞生长的细胞因子,还没有确凿的实验室证据确认不存在传染人的自体细胞的可能性,如存在副作用,可能导致不良后果;第四,这一技术实施过程中是否保证无菌、是否规范,目前都还没有制定相关的国家标准。
因此,专家建议爱美的人们,美容一定要选择有资质的美容机构,还要确定主治医生是否具有整形美容执业医生证书,自己要接受的美容技术是否经过了许可。此外,还要了解自己要接受的美容技术存在的不利因素。
多发性骨髓瘤
移植的时机
尽可能在“缓解”期(remission)内进行移植,是病患进行造血干细胞移植时的要求。缓解代表著病患体内癌细胞数目在经过治疗后,已经降低到某种标准以下,疾病暂时获得控制。因此在缓解期内进行移植,移植入的造血干细胞所新生成的免疫与造血系统较容易顺利成长、发挥正常功能,使疾病获得稳定控制并减少复发机会,以达成“长期缓解”或“痊愈”的治疗目标。相反的,当疾病治疗尚未达缓解时便进行造血干细胞移植,很容易出现移植失败状况与疾病复发现象。
干细胞的收集
不论是自体移植还是异体移植,都是从骨髓和周边血液收集干细胞。
1.骨髓的抽取

自体干细胞移植
自体干细胞移植
骨髓是骨骼内海绵状组织(就像羊猪骨头咬碎后,里面的软髓即是骨髓),通常位在大骨骼的骨骼腔中,於胸骨、颅骨、髋骨、肋骨和脊椎骨。人类成体以后,大部分的造血干细胞集中在骨髓,并分化再生成人体所需的血球与免疫系统,因此骨髓成为医界最早抽取造血干细胞的来源。
收集骨髓造血干细胞时,不论是自体病患或异体捐赠者的抽取方法皆相同。抽取的地点是在医院的手术房,让供髓者俯趴在手术台上,以全身麻醉的状态下进行。抽取骨髓时,并不需要进行皮肤切开以及缝合的手术,两位医师分别站在患者臀部左右两侧,利用抽取针头插入臀部两侧的肠骨内,抽取出红色黏稠的骨髓液(包含血浆、已分化或未分化之血球与造血干细胞)。抽取的骨髓液总量会根据受移植患者的体重,与供髓者骨髓内的细胞浓度而定(自体移植受移植者和供髓者就是同一个人了),大约是每公斤10~20C.C.,总量是600~1,500C.C.左右,占供髓者的2~5%的骨髓量(人体可於4周内再生补足所抽取的份量,所以不会减弱供髓者的免疫与造血功能)。
2.周边血液干细胞收集
正常生理状况下,血液中只含有非常微量的造血干细胞,数量不足提供移植之所需,但如果透过连续几天注射白血球生长激素(Granulocyte-ColonyStimulatingFactor,简称G-CSF),就可以将骨髓内之造血干细胞驱动(mobilize)至人体周边血液中,此时再经由血液分离的技术,就可取得所需之造血干细胞。
周边血是经由血液分离机取得,过程与分离式捐血相同,也不需要麻醉,只是需要先施打白血球生长激素,将骨髓内的造血干细胞驱赶至周边血液中,而后利用血液分离机以离心的方式,进行1~2次的白血球分离术以收集造血干细胞。
血液会从插在左手或右手手臂静脉的导管流进血液分离机,经过血液分离机以离心的方式将造血干细胞分离收集於机器内。分离干细胞后剩下的血液,将会立即从连在另一条手臂的导管回到体内。每次收集所需的时间约需3~6小时,一般需收集2~3次(即2~3天)。收集次数及收集量,主要是依据病患体重而定。收集后的成品保存於摄氏2~6度,如移植医院要求,可以室温保存,但须尽快植入病患体内,以不超过36小时为原则。若是自体移植者,收集到的周边血干细胞会被冷冻储存。
注:白血球生长激素是一种造血干细胞生长因子,能增加从骨髓释放到血管内的造血干细胞数量,以便透过血液分离的程序收集。
另外,白血球生长激素(G-CSF)还可应用在其他治疗上,例如癌症病患接受化学治疗后所造成的白血球减少、骨髓移植后所造成的白血球减少、特发性或周期性白血球减少、先天性白血球减少等等,可使用白血球生长激素增加其白血球的数目。
特别注意
自体干细胞移植后,因为超高剂量的化学治疗与放射线治疗难完全杀死骨髓瘤细胞,以致残余的癌细胞会导致病患再复发。复发后可以选择再次自体移植,这就是为什麼之前要收集足够进行两次移植的数量,或更多次数量的干细胞。若经过数次自体移植和药物治疗后,病情还是无法获得控制,可考虑异体干细胞移植,和其他尚在实验研究阶段的治疗方式。
案例
据英国《卫报》2011年3月30日报道,日本当局正在考虑从福岛第一核电站工人体内抽取骨髓,以获得干细胞。一旦工人因受辐射影响伤到骨髓,便可注入保存下来的自体健康干细胞,从而挽救勇士们的生命。[1]
《卫报》称,作为一项预防措施,该计划将有助于挽救奋不顾身战斗在核反应堆一线的工程师和注水工人。[2]
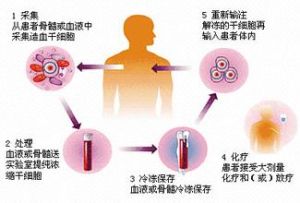
首先,工人们会被注入血液生长因子蛋白,促使骨髓产生更多造血干细胞并释放到血液中;其次,采集到的工人们的血液将通过“血液成分部分清除”疗法进行过滤,从中分离出干细胞;最后,血液会被输回体内,分离出的干细胞将被冷藏保存。一旦工人的骨髓因辐射受损,则可将事先冷藏的干细胞输入体内,从而重建免疫系统。密歇根大学综合癌症中心透露,这一过程称为“植入”,需要住院数周,并需要两三年时间恢复。
背景知识
造血干细胞具有干细胞强大的再生与分化的功能,它无时无刻的在生产人体所需的红血球、血小板和白血球。因为造血干细胞可分化红血球、白血球和血小板等,所以可用来治疗血液和免疫系统相关的疾病。造血干细胞存在於骨髓、婴儿脐带血及成人周边血液中。