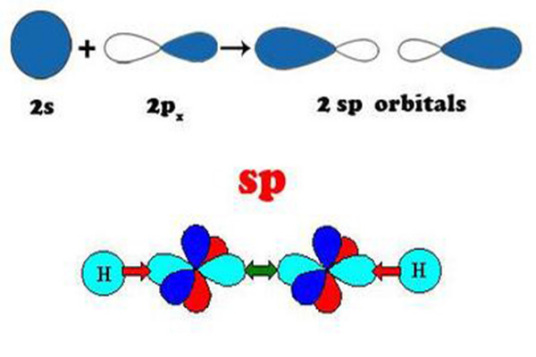
同一原子内由1个ns 轨道和1个np 轨道参与的杂化称为sp杂化 ,所形成的两个杂化轨道称为sp杂化轨道。每个sp 杂化轨道含有1/2的s成分 和1/2的p成分,杂化轨道间的夹角为180°。sp轨道杂化是基于轨道杂化理论的一个重要分支,是一种比较常见的轨道杂化方式。
精选百科
本文由作者推荐
sp杂化 相关的文章
白银时代项目位于云谷路1233弄,所在地块四面环路,将建成一个由办公、商业、住宅、轨道交通、配套公共设施等结合为一体的大型城市综合体,凸现城市快捷便利的交通生活空间和休闲娱乐氛围。
兜率宫坐落于仙岩极顶之上,它坐西朝东,五进而起,九根大柱支撑屋面,象征九五之尊的帝王宫殿,占地670平方米,高19米,彤壁朱扉,重檐丹楹,上覆灰色琉璃瓦,四周为花岗岩护栏,甚是庄严。北侧入宫,左右这副篆全楹联是:“自领名山司洞府,别开真境近人寰”,是出自元代文学家、翰林侍讲学士揭傒斯的《龙虎山》诗。正殿正中供奉道教教主老子像,像高12.3米,以应老子“道生一,一生二,二生三,三生万物”的哲学学思想。
是长江从南京以下至入海口的下游河段的旧称,流经江苏省、上海市。扬子江因古有扬子津渡口而得名,江阔水深浪大,受潮汐影响比较强烈。从镇江开始,长江进入三角洲河段,其中江阴以下为河口段,江面不断扩张成喇叭。长江在入海之前,接纳最后一条支流黄浦江。江宽水深,万吨海轮可以上溯到南京市。由于来华的西方传教士最先接触的是扬子江这段长江,听到的是“扬子江”这名称,西方把中国长江通称为“扬子江”,"Yangtze River"也成为长江在英语中的称呼。【概述图为南京长江第三大桥】
惠州市汽车客运站(Huizhou coach station)位于中国广东省惠州市惠城区,为一座国家一级公路汽车客运站,是惠州市内首座集长途汽车客运、城市公交站场以及城际铁路捷运为一体,同时兼顾休闲和商务的大型综合交通枢纽;车站隶属于惠州市汽车运输集团有限公司。惠州市汽车客运站始建于民国10年(1921年);于1963年7月1日移至惠州镇新建路77号;于1966年搬至惠州市佛祖坳;于2018年10月21日迁至惠城区天平山,改名为惠州市汽车客运南站。2019年2月27日,惠州市汽车客运南站更名回惠州市汽车客运站。
巴黎街头,永远风中凌乱的睡不醒头,似在诠释着法国女人独有的慵懒自由。无论是被经典的黑白灰、棕色、米色等中性色彩包裹,还是着一件基础款的T恤、风衣、大衣、衬衫,搭配一条图案色彩出挑的丝巾,法国女人也都能把上流社会的优雅气质信手拈来
天津市幼儿师范学校建立于1951年,是新中国建立的最早的幼儿师范学校之一,是天津市教委直属学校。2001年经天津市委、市政府决定天津幼师整建制组建天津师大学前教育学院。天津幼师招收外省市学生,天津师大学前教育学院招 收本市学前教育专业五年一贯制(初中毕业生)和两年制(三校生)学生。承担天津市幼儿师资(幼儿园园长、教师、保育员)培训任务。
簪中录》是侧侧轻寒创作的一部古代言情小说,由一段女宦官的爱恨情仇,牵引出步步大唐皇家惊心的秘案。在风起长安的段段情谜中,书中描写了女神探黄梓瑕眼中的大唐社会风情长卷,从被人诬陷的罪犯到夔王府的太监,通过调查案情终于洗清冤屈成为了夔王妃的曲折离奇经历。
地花生,中药名。为远志科植物西南远志Polygala crotalarioides Buch.-Ham.的根。分布于四川、云南等地。具有祛痰止咳,宁心安神,活血止痛之功效。常用于咳嗽咯痰不爽,心悸,失眠多梦。