生物学性状
形态与染色
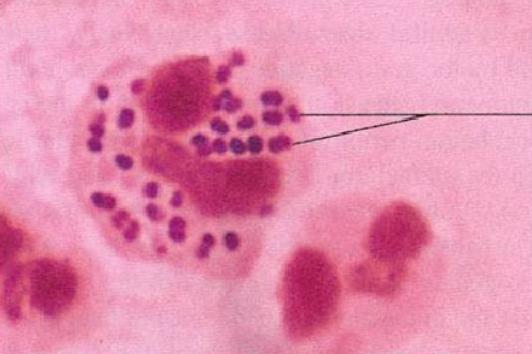
脑膜炎奈瑟菌为革兰染色阴性,常呈双排列,直径约为0.8μm的双球菌。单个菌体呈肾形。成双排列时,两个凹面相对。无鞭毛,不形成芽胞。有菌毛,新分离菌株有荚膜。
培养特性
专性需氧。营养要求高。最常用的培养基是巧克力色培养基。即将血液加热80℃后制成的血琼脂培养基。初次分离培养时,还需提供5%~10%的CO2气体。一般培养48小时后,脑膜炎奈瑟菌在培养基上形成圆形隆起、表面有光泽、透明或半透明、直径约1mm~5mm的露滴样粘液型菌落。无色素形成。血平板上无溶血现象。
生化反应
分解糖类产酸不产气。氧化酶试验阳性。脑膜炎奈瑟菌可产生自溶酶,人工培养时若不及时移种,数日后菌体自溶。
抗原构造及分类
1.荚膜多糖抗原(capsular polysaccharides antigen)具有群特异性。根据此抗原性不同,可将脑膜炎奈瑟菌分为至少13个血清群。与人类疾病关系密切的主要是A、B、C、Y及W-135群。A群及C群是引起脑膜炎流行的主要血清群。
2.外膜蛋白(outer membrane protein)具有型特异性。根据外膜蛋白不同将脑膜炎奈瑟菌分为20个血清型。2型和15型与流行性脑脊髓膜炎有关。外膜蛋白的功能是在细菌细胞壁上形成孔隙,有利于营养物质进入细胞内。
3.脂多糖抗原(lipopolysaccharide antigen,LPS)此抗原与大肠杆菌有共同抗原存在。脂多糖是脑膜炎奈瑟菌的主要致病物质。
抵抗力
脑膜炎奈瑟菌对外界环境的抵抗力弱。干燥、阳光、湿热及一般消毒剂很快将细菌杀死。本菌可产生自溶酶。体外25℃,碱性环境中很快导致菌体肿胀、裂解死亡。
致病性与免疫性
致病物质
1.荚膜:荚膜可抵抗宿主体内吞噬细胞的吞噬作用,增强细菌对机体的侵袭力。
2.菌毛:介导细菌粘附在宿主易感细胞表面,有利于细菌在宿主体内定居、繁殖。
3.内毒素:是脑膜炎奈瑟菌的主要致病物质。内毒素作用于小血管或毛细血管,引起血栓、出血,表现为皮肤出血性瘀斑;作用于肾上腺,导致肾上腺出血。大量内毒素可引起弥漫性血管内凝血(disseminated intravascular coagulation,DIC),导致休克,预后不良。
所致疾病
流行性脑脊髓膜炎(简称流脑)是由脑膜炎奈瑟菌(Nm)通过呼吸道传播引起的化脓性脑膜炎。
人类是脑膜炎奈瑟菌唯一的易感宿主。细菌由鼻咽部侵入机体,依靠菌毛的作用粘附于鼻咽部粘膜上皮细胞表面。多数人感染后表现为带菌状态或隐性感染,细菌仅在体内短暂停留后被机体清除。只有少数人发展成脑膜炎。我国引起脑膜炎的主要是A群菌,B群常为带菌状态。脑膜炎奈瑟菌感染的发病过程可分为3个阶段:
①病原菌首先由鼻咽部侵入,依靠菌毛吸附在鼻咽部粘膜上皮细胞表面,引起局部感染;
②随后细菌侵入血流,引起菌血症,伴随恶寒、发热、呕吐、皮肤出血性瘀斑等症状;
③侵入血流的细菌大量繁殖,由血液及淋巴液到达脑脊髓膜,引起脑脊髓膜化脓性炎症。患者出现高热、头痛、喷射性呕吐、颈项强直等脑膜刺激症状。严重者可导致DIC,循环系统功能衰竭,于发病后数小时内进入昏迷。病理改变表现为脑膜急性化脓性炎症伴随血管栓塞,白细胞渗出。
免疫性
机体对脑膜炎奈瑟菌感染的免疫力主要依赖于体液免疫。显性感染、隐性感染或疫苗接种2周后,血清中群特异性IgG、IgM和IgA抗体水平明显升高。分泌型IgA抗体可阻止脑膜炎奈瑟菌侵袭呼吸道粘膜上皮细胞;血清IgG及IgM抗体在补体的参与下有杀死病原菌的作用;血清抗体在补体的参与下可增强吞噬细胞对病原菌的吞噬与杀灭。6个月内的婴儿可通过母体获得IgG抗体,产生自然被动免疫,故很少发生感染。6个月后,来自母体的抗体水平逐渐下降,婴儿对疾病的易感性逐渐增强,故6月~2岁年龄组婴儿免疫力最低,是脑膜炎奈瑟菌的易感人群。
微生物学检查法
标本
取患者脑脊液或刺破皮肤出血瘀斑取渗出物作涂片或培养。血液标本作培养。带菌者检测可取鼻咽拭子。
直接涂片镜检
脑脊液离心沉淀后,取沉淀物涂片,革兰染色后镜检。或消毒患者皮肤出血瘀斑处皮肤,用无菌针头挑破瘀斑取渗出物制成涂片,革兰染色后镜检。如镜下见到中性粒细胞内、外有革兰染色阴性双球菌时,即可作出初步诊断。
分离培养与鉴定
血液与脑脊液标本在血清肉汤培养基中增菌后,接种到巧克力色血琼脂平板上,置于含5%~10%CO2的环境中孵育。挑取可疑菌落涂片镜检,并作生化反应(表13-1)及型特异性多价血清的凝集试验鉴定。
生化鉴定
主要通过氧化酶、糖类发酵以及培养生长特点进行。
①细菌形态呈肾形;
②氧化酶试验阳性;
③触酶试验阳性;
④分解葡萄糖、麦芽糖产酸不产气;
⑤荚膜多糖抗原直接凝集试验。
血清凝集法
根据荚膜多糖可将脑膜炎奈瑟氏菌分为A、B、C、D、X、Y、Z、29E、W135、L、H、I、K等13个血清群,其中A、B、C群最为多见,约占90%。
关于血清凝集法用的诊断血清方面,推荐天津生物芯片公司生产的脑膜炎奈瑟氏菌全套诊断血清产品。这套产品除了包含脑膜炎奈瑟氏菌菌10个常见血清群的诊断血清。
核酸扩增法
流行性脑膜炎的临床诊断通常以出现发热、呕吐、头痛等临床症状为依据。进一步的确诊则需在病人脑脊液或急性衄液中分离到脑膜炎双球菌。但分离培养方法的检出阳性率较低.并且至少需要2~3d才能确诊感染.这对疾病的及时治疗极为不利。此外,受抗生素使用及其他非特异性因素的影响.分离培养法的灵敏度不高.极大地降低了诊断结果的可靠性。因此,寻找一种快速、灵敏并且适用于I临床诊断的检测方法已显得非常莺要。近年来,因为具有特异性好、灵敏度高、检测周期短等优点,在PCR的基础上建立的基因诊断技术已广泛应用于多种病原微生物的临床检测。四川大学华西公共卫生学院联合四川省疾病预防控制中心以PCR技术为基础,结合我国流脑的流行现状,建立了Nm ABC群的快速诊断方法。
核酸扩增技术,即聚合酶链式反应(polymerase chainreaction,PCR),其基本原理是设计、合成两条寡核苷酸,作为引物,对应于待测病原微生物某一段特异性序列的两端,然后在体外模拟DNA体内复制的过程反复扩增,使靶序列放大上万倍甚至上百万倍而被检测出来。
快速诊断法
依据是脑膜炎患者脑脊液及血清中存在脑膜炎奈瑟菌可溶性抗原。因此可采用已知的抗体检测有无相应的抗原。
1.对流免疫电泳:此法较常规培养法敏感,特异性高。一般1小时内即可得到结果。
2.SPA协同凝集试验:将待检的患者脑脊液或血清与已知脑膜炎奈瑟菌IgG类抗体标记的产生SPA的金黄色葡萄球菌混合。若标本中存在脑膜炎奈瑟菌的可溶性抗原,则使抗体标记的金黄色葡萄球菌聚集在一起,形成肉眼可见的凝集现象。
防治原则
预防脑膜炎奈瑟菌感染的关键是要尽快消除传染源、切断传播途径及提高人群免疫力。
我国1980年正式使用A群多糖菌苗,临床观察表明对学龄儿童和成人保护率可达90%。但此种疫苗对2岁以下婴幼儿免疫原性差,其一是因为脑膜炎荚膜多糖抗原属于T细胞非依赖抗原,免疫效果与接种者年龄有明显的依赖关系;其二,多糖菌苗诱导机体产生的IgG抗体主要为IgG2亚类,出现较迟,一般到8~12岁才能上升至成人水平。因此,婴幼儿接种多糖菌苗后往往以产生短暂的IgM抗体为主。国外采用A群和C群多糖与白喉毒素蛋白偶联的偶联菌苗接种8~10周龄的婴儿,证明这种偶联菌苗具有良好的免疫原性及安全性。
流脑的治疗首选药物为青霉素G,剂量要大。对青霉素过敏者,可用氯霉素或红霉素。