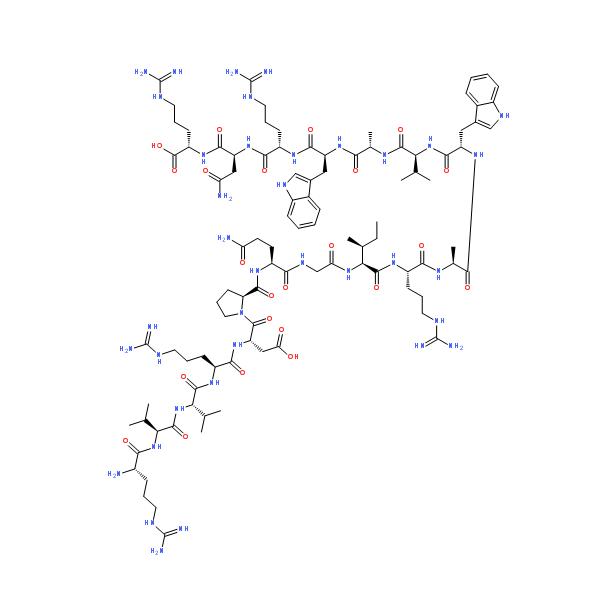
溶菌酶主要通过破坏细胞壁中的N-乙酰胞壁酸和N-乙酰氨基葡萄糖之间的β-1,4糖苷键,使细胞壁不溶性黏多糖分解成可溶性糖肽,导致细胞壁破裂内容物逸出而使细菌溶解。溶菌酶还可与带负电荷的病毒蛋白直接结合,与DNA、RNA、脱辅基蛋白形成复合体,使病毒失活。该酶广泛存在于人体多种组织中,鸟类和家禽的蛋清、哺乳动物的泪、唾液、血浆、乳汁等液体,以及微生物也含此酶,其中以蛋清含量最为丰富。其中根据其来源的不同,可以将其分为四类,分别是植物溶菌酶、动物溶菌酶、微生物溶菌酶以及蛋清溶菌酶。
精选百科
本文由作者推荐
溶菌酶 相关的文章
2019年7月4日6点30分,浙江省杭州市淳安县租客梁某华、谢某芳谎称带孩子赴上海喝喜酒,将房东9岁女童章子欣从家中带走。7月7日,梁某华、谢某芳未按约定带回孩子,之后失去联络。
《暗黑破坏神IV》(Diablo IV)是暴雪娱乐公司开发的一款动作角色扮演游戏。该作是系列游戏《暗黑破坏神3》的续作。该作时间线为《暗黑破坏神3:夺魂之镰》结束后的几十年。
塞外古代指长城以北的地区,也称塞北。包括内蒙古、甘肃、宁夏、河北等省、自治区的北部以及蒙古高原,塞外政治军事文化中心和林。雍正皇帝:“中国之一统,始于秦;塞外之一统,始于元;而极盛于我朝,自古中外一家,幅员极广,未有如我朝者也”。
东北梅花鹿头俊秀,耳大、灵活,躯干紧凑,四肢匀称、细长,主蹄狭尖。东北梅花鹿初角茸平均干重25-30克,若在初角茸长至5-6厘米时锯下1.5-2.0厘米(俗称“破茬”),还能生长分杈的初角茸,干重可达150-200克。公鹿的活重、屠宰率、净肉率和出肉量分别为130-140千克、55.0-64.1%、50-55%和65-75千克;母鹿相应为65-85千克、51-54%、38-43%和25-35千克。由于东北梅花鹿数量大,繁殖力高,茸色茸型多呈显性遗传,并且经多年的人工选育,茸高产质优,耐粗饲和适应性、生活力、抗病力强,可作为品种间杂交优良的父本或母本。
智能网联汽车,(IntelligentConnectedVehicle,ICV),是指车联网与智能车的有机联合,是搭载先进的车载传感器、控制器、执行器等装置,并融合现代通信与网络技术,实现车与人、路、后台等智能信息交换共享,实现安全、舒适、节能、高效行驶,并最终可替代人来操作的新一代汽车。
大召寺是中国内蒙古呼和浩特玉泉区南部的一座大藏传佛教寺院,属于格鲁派(黄教)。大召寺其中“召”为藏语寺庙之意。汉名原为“弘慈寺”,后改为“无量寺”。因为寺内供奉一座银佛,又称“银佛寺”。大召寺是呼和浩特最早建成的黄教寺院,也是蒙古地区仅晚于美岱召的蒙古人皈依黄教初期所建的大型寺院之一,在蒙古地区有大范围的影响。
pvc名片主要是用一种乙烯基的聚合物质的材料为载体,采用丝网印刷技术,结合烫电化铝等工艺制作出的一种特殊的名片。从广告心理学家认为,第一印象对于商务洽谈起着决定性的作用,选择名片也成为众多商务人士的烦恼,一张质地优良色彩表现力强具有坚韧品质的名片犹如一个人的性格展示,因而现在大家都在渐渐的对PVC卡片材料重视起来。

王老师
还来不及增加介绍呢!
作者